マルチモードサンプル導入システム(MSIS)
MSIS は、複数の水素化物発生元素の超低微量元素濃度を同時に測定するために、ICP-OES 装置とともに使用されます。MSIS は、サンプルと液体試薬の両方を一緒に混合します。気体の反応産物は窒素流によって ICP-OES 内に掃出されます。
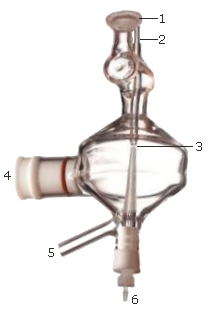
部品は次のとおりです。
|
1 |
トーチクランプでトーチに固定されたボールジョイント |
|
2 |
上部の溶液導入部 |
|
3 |
上部と下部の溶液導入部チューブ間の 1 ~ 3 mm の隙間 |
|
4 |
ネブライザー用ソケット |
|
5 |
ドレイン |
|
6 |
下部の溶液導入部 |
はじめに
MSIS は噴霧と水素化物発生機能の両方を組み合わせ、従来のスプレーチャンバとしても水素化物発生装置としても操作できます。揮発性気体水素化物を分離し、分析対象元素を濃縮することにより、干渉を低減さらには除去します。
動作モード
従来の噴霧モード
スプレーチャンバの上部と下部の両方に接続されたポンプチューブを遮断します。溶液とガスがネブライザーを通じて導入されます。
水素化物発生モード
溶液は下部からポンプ移送され、還元剤は上部からポンプ移送されます。溶液は、上部と下部のチューブの間にある 1 ~ 3 mm の隙間で混合します。ネブライザーのポンプチューブは遮断されています。
デュアルモード
MSIS は、ネブライザーモードと水素化物発生モードを組み合わせて動作します。サンプルは、ネブライザー内とスプレーチャンバの下部ポート内の両方にポンプ移送されます。還元剤はスプレーチャンバの上部ポート内にポンプ移送されます。下部ポートから導入された溶液は、溶液導入チューブ間の隙間で還元剤と混合され、水素化物を生成します。
設置
MSIS の設置方法:
- MSIS に付属の説明書に従って、フィッティングとチューブを MSIS に接続します。
- スプレーチャンバのソケットにネブライザーを挿入します。
- MSIS は、トーチのボールジョイント側の端部にトーチクランプで取り付けます。
- 溶液の移送と、チャンバからの廃液のポンプ排出用に、5 チャンネルのペリスタルティックポンプにチューブを接続します。
操作
一般的な手順
このテクニックでは、分析結果の真度と精度に影響を与えるすべての活動において特別に高い配慮が要求されます。すべての実験室の手順において厳密な清浄度が不可欠です。標準液とサンプルは綿密に調製し、注意深く取り扱う必要があります。器具の汚染を防ぐために厳格な注意を払う必要があります。実験室の器具が理想的な条件で保管されているときも、使用前に入念に再洗浄する必要があります。
すべての試薬と蒸留水の汚染防止にも厳格な注意を払う必要があります。試薬に分析対象元素がまったく含まれていないことが理想的です。しかし、すべての試薬中のすべての分析対象元素で実現するのは明らかに不可能です。したがって、試薬中の分析対象物に帰する分析シグナルのレベルを常に確立しておく必要があります。標準的な方法では、装置を較正し分析プログラムを実行する前に、ブランク溶液からの分析シグナルを確認します。しかし MSIS では、この手順を拡大して、システムにポンプで流す酸と水素化ホウ素ナトリウム溶液を含める必要があります。
廃液は、適切な安全慣行と地域の政府規制に従って処理してください。
標準液の調整
1000 mg/mL ストック溶液から較正標準液を調製します。
一部のサンプルについては、標準添加法を使用して取得した通常の検量線メソッドを使って較正スロープを比較する必要があります。スロープが同一でない場合、分析に標準添加法を使用する必要があります。
還元剤—水素化ホウ素ナトリウム
水素化ホウ素ナトリウム(NaBH4)の推奨濃度は 0.6% w/v です。ただし、高濃度の金属を含む困難なサンプルでは、水素化ホウ素ナトリウム濃度を 0.3% w/v まで下げるとより良好な結果が得られます。
 |
水銀の測定には塩化スズの還元剤を推奨します。水銀を参照してください。 |
必ず水酸化ナトリウム(NaOH、0.5% w/v)を最初に添加して溶液を安定化させてください。水素化ホウ素ナトリウムは 1 ~ 2 日で顕著に分解されるため、一度に 500 mL 以上を調製しないでください。この量は、約 1 mL/分の流量で、一般的な就業日 1 日分の連続操作に十分です。5 ミクロンフィルターで溶液をろ過することにより安定性が向上する可能性があります。5 ℃ で保管することによっても溶液の使用可能期間を伸ばすことができます(5 ℃ で保管した場合、溶液は約 1 週間安定性を維持します)。分析前に、溶液を室温に戻してください。
ポンプチューブ
ポンプチューブは、流量を確認することによって定期的にチェックする必要があります(ポンプの調整を参照)。
 |
最初に高濃度の酸を酸チューブに流すと、チューブの内側が白くなることがありますが、これによりチューブの効率が低下することはありません。 |
分析前にサンプル、試薬、標準液のすべてが室温になっている必要があります。ポンプ流量は溶液の温度で変動することがあるため、ICP-OES ペリスタルティックポンプは低温または高温の溶液では正しく動作しません。
基本的なメソッド
水素化物を生成する元素は、サンプルおよび標準液中で複数の酸化状態で存在することがあります。サンプルと標準液が正しい酸化状態で存在することを確実にするために、サンプルと標準液用に、次の分析メソッドを作成しました。
 |
従来は、還元剤に 1% ヨウ化カリウム(KI)を含める慣行が推奨されていました。過去に、分析前の還元ステップでサンプルに 1% KI を添加した場合、より良好な結果が得られることが示されていました。現在、還元剤に KI を添加することは推奨されなくなりました。 |
アンチモン
少なくとも 1 M の塩酸(HCl)でサンプルを調製し、Sb(V)として存在する分析対象物がすべて、1% w/v の濃度のヨウ化カリウムの作用によって Sb(III)に還元されることを確認します。還元は自発的であり、加熱は不要です。
| 還元剤コンテナ: | NaBH4 0.6%、 NaOH 0.5% |
| 酸コンテナ: | 5~10 M HCl |
ヒ素
 |
追加注意事項も参照してください。 |
サンプル中のヒ素は無機形態でなければなりません。無機形態でないときは、分解が必要になります。
分解が必要なときは、酸分解(酸化性酸の残留物が存在しないことを確認する)または適切な灰化補助剤による灰化を使用してください。単純な乾式灰化が推奨されます。
サンプルを少なくとも 1 M の塩酸(HCl)で調製します。
As(V)として存在する分析対象物がすべて、1% w/v の濃度のヨウ化カリウムの作用によって As(III)に還元されることを確認します。
還元は室温で約 50 分かかります。還元は 70 ℃ で約 4 分間行うこともできます。しかし、分析前にサンプルと標準液を室温に冷却する必要があります。ポンプ流量は溶液の温度で変動することがあるため、ICP-OES ポンプは、高温の溶液では正しく動作しません。
還元ステップを省略し、分析対象物を As(V)として保持したときは、分析感度が As(III)で得られる感度の約 20~30% になります。元の溶液に As(III)が含まれるときは、ヨウ化カリウムによる還元は不要です。
| 還元剤コンテナ: | NaBH4 0.6%、 NaOH 0.5% |
| 酸コンテナ: | 5~10 M HCl |
ビスマス
ヨウ化カリウムが存在すると分析反応が著しく抑制されます。ビスマスの測定を実施する前に、MSIS にヨウ化カリウムが完全に存在しないことを必ず確認してください。
 |
汚染を避けるために、KI–As、Sb、Se を使用した予備還元を必要とする元素の分析専用に、別個のサンプル導入システムを設けることが推奨されます。 |
1 M の塩酸(HCl)でサンプルを調製します。
| 還元剤コンテナ: | NaBH4 0.6% NaOH 0.5% |
| 酸コンテナ: | 5 M HCl(これより高濃度の酸では分析シグナルが抑制されます) |
水銀
微量のヨウ化カリウムが水銀の蒸発生成に著しく干渉し、分析反応が完全に抑制されることがあります。水銀の測定を実施する前に、MSIS にヨウ化カリウムが完全に存在しないことを必ず確認してください。
 |
汚染を避けるために、ヨウ化カリウム(KI)を使用した予備還元を必要とする元素の分析専用に、別個のサンプル導入システムを設けることが推奨されます。 |
サンプル中の水銀は無機形態でなければなりません。無機形態でないときは、分解または干渉抑制剤(たとえば、CdCl2)の使用が必要になります。
分解が必要な場合は、酸分解または適切な灰化補助剤による灰化を使用してください。水銀が損失するため、単純な乾式灰化は推奨されません。
希釈した水銀溶液は不安定になりやすくなります。分析溶液はすべて硝酸(5% v/v)と塩酸(5% v/v)を添加して安定化させる必要があります。新鮮な標準液を毎日調製してください。
水銀は、還元剤として塩化スズを使用して測定することを推奨します。
| 還元剤コンテナ: | HCl(20% v/v)中の SnCl2(25% w/v) |
| 酸コンテナ: |
H2O |
 |
SnCl2 溶液を調製するには、濃縮 HCl を直接固体の SnCl2 に添加し、混合物をホットプレートで加温して完全に溶解してから水を加えます。 |
 |
水銀はプラスチックに付着するため、メモリ現象の影響を受けます。これらのメモリ現象の影響を最小限に抑えるため、濃度を低く保ってください。 |
このメソッドでは、水素化物を生成する元素で通常使用する濃度よりも、低い濃度の水素化ホウ素ナトリウムを使用することが推奨されます。MSIS にポンプ送出する酸の濃度は一般的に重要ではありません。
水銀分析対象物の損失を防ぐため、スプレーチャンバのドレインがクランプ留めされていることを確認します。
| 還元剤コンテナ: | NaBH4 0.3% NaOH 0.5% |
| 酸コンテナ: | 5 M HCl |
このメソッドで得られる分析シグナルは、塩化スズのメソッドよりも低いことがあります。注意してください。
セレン
 |
追加注意事項も参照してください。 |
サンプル中のセレンは無機形態でなければなりません。無機形態でない場合は、分解が必要になります。
分解が必要な場合は、酸分解または適切な灰化補助剤による灰化を使用してください。セレンは揮発性が高く回収率が不良であるため、単純な乾式灰化は推奨されません。
Se(VI)は水素化物生成によって定量的に回収されないため、濃縮塩酸で加温することにより Se(IV)に還元する必要があります。6 ~ 7 M の塩酸(これより低い酸濃度を使用すると元素間の干渉が大きくなります)でサンプルを調製し、少なくとも約 10 分間 70 ~ 90 ℃ で加熱します。分析前に室温まで冷却してください。
| 還元剤コンテナ: | NaBH4 0.6% NaOH 0.5% |
| 酸コンテナ: | 10 M HCl |
テルル
ヨウ化カリウムが存在すると分析反応が著しく抑制されます。テルルの測定を実施する前に、MSIS にヨウ化カリウムが完全に存在しないことを必ず確認してください。
 |
汚染を避けるために、ヨウ化カリウム(KI)を使用した予備還元を必要とする元素の分析専用に、別個のサンプル導入システムを設けることが推奨されます。 |
Te(IV)は水素化物生成によって定量的に回収されないため、Te(IV)に還元する必要があります。6 ~ 7 M の塩酸でサンプルを調製し、少なくとも約 10 分間 70 ~ 90 ℃で加熱し、分析前に室温まで冷却します。
| 還元剤コンテナ: | NaBH4 0.6%、 NaOH 0.5% |
| 酸コンテナ: | 5 M HCl |
スズ
スズの最良の結果は、一般的に 1% 酒石酸で調製された溶液で得られます。また、ある試験では L-システインを添加すると水素化物生成によりスズの測定が大きく改善することが示されています。2 L-システインにより金属の干渉が低減され、精度と感度が向上します。検量線の直線性における、ある程度の改善も認められています。
スズの測定において、MSIS 内にポンプで送出される酸の濃度も重要です。0.5 M を超える濃度では分析シグナルが著しく低下します。
| 還元剤コンテナ: | NaBH4 0.6%、NaOH 0.5% |
| 酸コンテナ: | 0.5 M HCl |
| サンプル: | 1% 酒石酸、pH 制御(2.0 ~ 3.0) |
代替メソッド
| 還元剤コンテナ: | NaBH4 0.5%、NaOH 0.1% |
| 酸コンテナ: | D.I.H2O |
| サンプル: | 1% HNO3, 1% L-システイン |
追加補足
- ヒ素とセレンの両方を同じサンプルで測定するときは、セレンを最初に測定し、サンプルまたは標準液中にヨウ化カリウム(KI)が存在しないようにしてください。その後、KI の還元ステップとその他の適切な処理(例えば、過度の硝酸が存在するときの尿素の添加)の後に、ヒ素を測定できます。
- 鉄やニッケルといった高濃度の金属を含む多くの実用的なサンプル中のヒ素とセレンを測定する際に、0.3% w/v の NaBH4 溶液濃度を使用すると(0.6% w/v ではなく)、干渉がより低くなることが認められています。ただし、低濃度の還元剤を使用するほど、感度が低くなることがあります。
- ヒ素とセレンへのコバルト、銅、鉄、ニッケルなどの遷移金属の干渉は、サンプルを 6~7 M の HCl で調製することにより最小限に抑えることができます。酸濃度が低いほど、元素間の干渉が大きくなります。
- ランタン化合物を使用した共沈法も有用であることが確認されています。
参考文献
- Smith, A.E., ‘Interferences in the determination of elements that form volatile hydrides with NaBH4 using AAS and Ar/H2 flame.’, Analyst, May, 1975, 100, 300–6.
- AA Application Note, 1992, October, No. 107.
追加の参考文献
AA Application Notes, Numbers, AA: 38, 44, 50, 51, 56, 60, 65, 78, 82, 86, 87, 105, 107 (available for download from the Agilent Technologies website at www.agilent.com)
Spectroscopy, 1985, 1(0), 60
Applied Spectroscopy, 1985, 39(1), 48
チューブのメンテナンス
ポンプチューブ
システムを使用していないときは、ポンプの圧力バーを開放し、チューブをローラー周辺から取り外し、リテーニングブラケットから取り外す必要があります。これにより、チューブのゆがみが最小限に抑えられ、使用可能期間の延長に役立ちます。
ポンプチューブの機械的摩耗を減らすには、チューブの外側とポンプローラーの表面にシリコン潤滑剤で毎日スプレーします。
すべてのポンプチューブの効率は、最終的には交換が必要になるまで低下します。各ポンプチューブの性能を流量の測定によって定期的にモニタリングする必要があります(ポンプの調整を参照)。このモニタリングの結果が許容できなくなったら、速やかにポンプチューブを廃棄してください。
 |
黒/黒ポンプチューブからペリスタルティックポンプに接続しているチューブは、交換が必要になることが時折あります。交換するには、付属の黒いフッ素エラストマーチューブを長さ 2 cm に 4 本切断します。2 本の黒/黒ポンプチューブの各終端に、2 cm に切断したフッ素エラストマーチューブを配置します。 |
フッ素エラストマーチューブ
ガス/液体セパレーターからネブライザーに接続するフッ素エラストマーチューブは、ヨウ化カリウムによる汚染の影響を特に受けやすくなっています。この状況を回避するには、ヨウ化カリウム(KI)を使用した予備還元を必要とする元素の分析専用に、別個のサンプル導入システムを設けることが推奨されます。
フッ素エラストマーチューブの洗浄手順を以下に示します。
KI の汚染がないときは、蒸留水でよく洗い流すことによりチューブを洗浄できます。
KI の汚染があるときは、以下の手順に従って KI の痕跡を除去する必要があります。
- チューブを外して取り除きます。
- チューブを水酸化ナトリウム溶液(0.5% w/v)に浸漬します。希釈塩酸で十分に洗浄してから、蒸留水でしっかりと洗浄します。
- ほこりのない場所でチューブを自然乾燥させます。
- チューブを元のとおり接続します。
チューブとガス/液体セパレーターからヨウ素の痕跡を除去する別の方法は、5 ~ 10 分間、新しく調製した 1% チオ硫酸ナトリウム溶液をポンプでシステムに流すことです。その後、蒸留水を 5 ~ 10 分間システムにポンプで流して、チオ硫酸を除去する必要があります。