设置和运行具有扩展 QC 或具有 USP 232/233 和 ICH Q3D 支持的扩展 QC 的方法
单击 File > Options > Expanded QC(文件 > 选项 > 扩展 QC)配置设置,以验证并运行符合《美国药典》(USP) <232>/<233> 和国际协调委员会 (ICH) Q3D 要求的方法。
 |
需要管理员权限才能更改扩展 QC 和 USP 233/ICH Q3D 设置。 |
有关如何设置扩展 QC 运行或具有 USP <232/233> 和 ICH Q3D 要求的扩展 QC 运行的详细信息,请查看以下视频。
扩展 QC
在选项页面上启用扩展 QC 功能
单击 File > Options > Expanded QC > Enable expanded QC functionality(文件 > 选项 > 扩展 QC > 启用扩展 QC 功能),将样品和默认所有样品 QC (ASQC) 级别添加到 QC 表中。此操作用于比较样品与预期分析物水平。
在选项页面上创建样品类型
要查看演示,请在“设置和运行具有扩展 QC 的方法”视频中单击“启用和配置扩展 QC”。
- 输入样品类型名称,然后单击 + 按钮。
- 对所有样品类型重复上述操作。
- 根据样品中元素的预期范围输入 QC 限值。
- 单击 OK(确定)。
在 QC 页面上选择 QC 测试
要查看演示,请在“设置和运行具有扩展 QC 的方法”视频中单击“设置 QC 测试”。
对工作表中具体的、可由用户定义的样品类型的所有样品,评估其所有样品 QC 定义 (ASQC)。
如果样品类型为“All-Samples”(所有样品)(在 Sequence(序列)页面上定义),则无论选择了何种样品类型,都将根据此 QC 定义评估序列表中的所有样品。
如果更改了样品类型(图 1),则还必须在 Sequence(序列)页面(图 2)上更改样品类型,才能将此 QC 定义应用于样品。
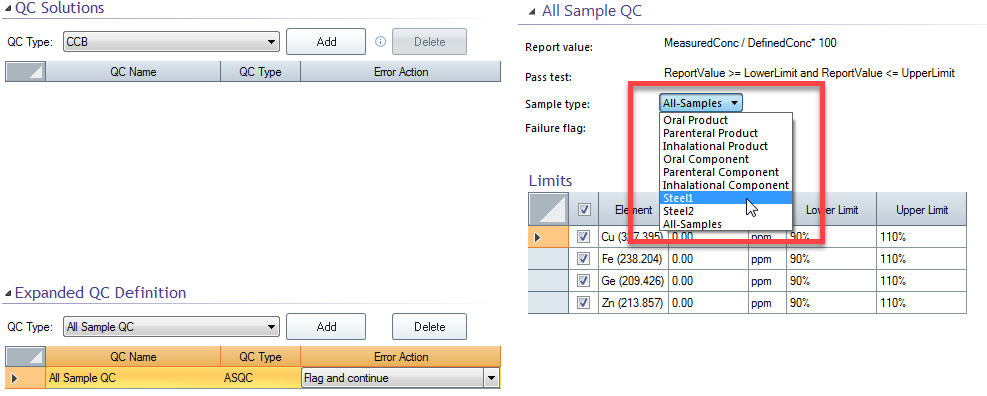
图 1.在 File > Options > Expanded QC(文件 > 选项 > 扩展 Qc)页面上创建 Steel1 样品后,在 QC 页面上选择 Steel1。
在序列页面上选择样品类型
有关如何添加 QC 类型和更改样品类型的演示,请在“设置和运行具有扩展 QC 的方法”视频中单击“设置序列”。
- 可通过添加或删除额外的样品数据列来自定义视图和报告。
- 选择样品类型以与在 QC 页面中创建的特定 QC 定义相关联。
无论在 Sequence(序列)页面中选择了何种样品类型,具有“All-samples”(所有样品)样品类型的 QC 定义将应用于序列中的所有样品。
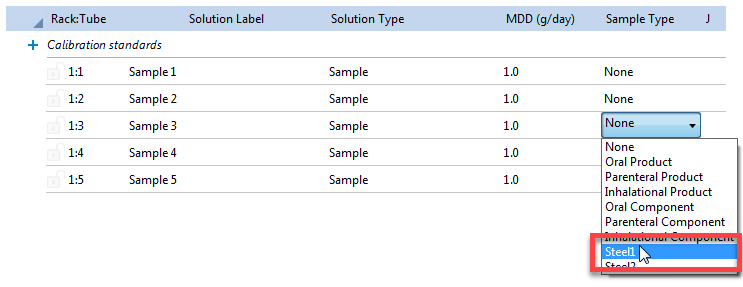
图 2.在 Sequence(序列)页面上选择样品类型。
设置具有 USP 和 ICH 要求的扩展 QC 的方法
 |
需要管理员权限才能更改扩展 QC 和 USP 232/233 和 ICH Q3D 设置。 |
在选项页面上启用 USP 232/233 和 ICH Q3D 的特定支持
单击 File > Options > Expanded QC > Enable USP 232/233 and ICH Q3D-specific support(文件 > 选项 > 扩展 QC > 启用 USP 232/233 和 ICH Q3D 的特定支持),在表中填充 USP232 和 ICH 每日允许暴露限量 (PDE) 级别,并在工作表中启用 USP232 和 ICH 的特定 QC。
 |
有关定义和要求的详细信息,请访问 USP (http://www.usp.org) 和 ICH (www.ich.org) 网站。 |
所有测试均预先填充来自 USP 232/233 和 ICH Q3D 方法验证测试限值的推荐值。限值是可编辑的。
添加样品类型或更改 PDE 值
- 输入名称,然后单击 Add(添加)(加号)图标以添加样品类型或更改现有的 PDE 值(如果选择了“Enable USP 233/ICH Q3D specific support”(启用 USP 233/ICH Q3D 的特定支持))。
- 输入或编辑每日允许暴露限量。
要删除样本类型,请在表中选择适当的列,然后单击 Remove(删除)(减号)图标。
借助扩展 QC,可以选择标准 QC 定义帮助验证和运行遵循 USP <232/233> 和 ICH Q3D 要求的方法,并将其分配给特定的样品类型。
根据“J”值分配合格/不合格。
“J”值根据特定药物的 MDD(每日最大剂量)、样品前处理参数(重量、体积和稀释倍数),并结合每种分析元素的 PDE 计算得到。
在 QC 页面上选择 QC 测试
添加 USP 232/233 和 ICH Q3D 支持时,这些公式不可编辑,并且要根据 USP <232/233> 和 ICH Q3D 要求定义。
除“LSpike”外,唯一可用的错误标记是“Flag and continue”(标记并继续)。
所有定义限值都预先填充了建议的 USP 和 ICH 要求,但是它们是可编辑的。
 |
有关定义和要求的详细信息,请访问 USP (http://www.usp.org) 和 ICH (www.ich.org) 网站。 |
关于 USP 232/233 和 ICH Q3D QC 类型
成分
求和选项可测量药物成分(原料、赋形剂和 API)中的杂质,并根据药物成分中的杂质含量和药品中每种成分的百分比来计算药品中的元素杂质。
控制阈值
选择以检查元素杂质水平是否低于控制阈值(定义为药品中已确定的 PDE 的 30%)。如果检查表明元素杂质水平高于控制阈值,则应建立其他控制措施以确保元素杂质水平不超过药品中的 PDE。
有关设置 Lspike 并使用加标计算器的示例,请在“具有 USP 232/233 和 ICH Q3D 要求的扩展 QC”视频中单击“设置 QC 测试”。
Lspike 是 J 值*的加标百分比。常用 50%、100% 和 150% 的 J 加标;但是最多可以选择 8 个加标水平。加标数(加标水平)在 File > Options > Expanded QC(文件 > 选项 > 扩展 QC)页面中设置。
加标计算器 (在限值表旁)确定用于不同百分比的 J 的加标所需要的浓度。给定溶液的实际浓度“1.00J”取决于样品制备时特定药物的重量、体积和稀释倍数,以及最大每日剂量和给药途径。
(在限值表旁)确定用于不同百分比的 J 的加标所需要的浓度。给定溶液的实际浓度“1.00J”取决于样品制备时特定药物的重量、体积和稀释倍数,以及最大每日剂量和给药途径。
* J 值定义为目标浓度下目标元素的 PDE 浓度(经过适当稀释后处于仪器工作范围内)。
产品
药品选项可测量药品中每种元素的含量,并将按比例缩放至最大日剂量的结果与修改后的日剂量 PDE 进行比较。按比例缩放至最大日剂量的每种元素杂质所测得的量不得超过规定的 PDE。
限值
USP 和 ICH 设置的建议限值是预先填充的,但可以编辑。
在序列页面上选择样品类型
有关如何添加 QC 类型和更改样品类型的演示,请在“具有 USP 232/233 和 ICH Q3D 要求的扩展 QC”视频中单击“设置序列”。
- 可通过添加或删除额外的样品数据列来自定义视图和报告。
- 选择样品类型以与在 QC 页面中创建的特定 QC 定义相关联。
无论在 Sequence(序列)页面中选择了何种样品类型,具有“All-samples”(所有样品)样品类型的 QC 定义将应用于序列中的所有样品。

图 2.在 Sequence(序列)页面上选择样品类型。
有关如何设置扩展 QC 运行或具有 USP <232/233> 和 ICH Q3D 要求的扩展 QC 的详细信息,请查看以下视频。
另请参见: